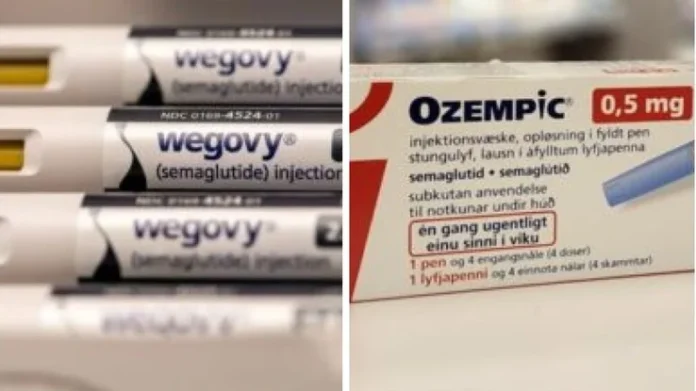
Medida da Anvisa visa combater uso indiscriminado e exige controle rigoroso na venda de medicamentos à base de agonistas GLP-1
Desde esta semana, farmácias e drogarias em todo o país passaram a reter as receitas de medicamentos conhecidos como canetas emagrecedoras, como Ozempic, Mounjaro e Wegovy, utilizados no tratamento de diabetes e obesidade. A medida passou a valer 60 dias após a decisão da diretoria colegiada da Agência Nacional de Vigilância Sanitária (Anvisa), tomada em abril, e representa um novo marco no controle da prescrição e dispensação desses fármacos.
A partir de agora, a venda só será permitida com prescrição médica em duas vias, sendo uma delas retida no estabelecimento, assim como já ocorre com antibióticos. As receitas terão validade de até 90 dias e farmácias deverão registrar toda a movimentação desses produtos no Sistema Nacional de Gerenciamento de Produtos Controlados (SNGPC).
Riscos e uso indevido
A decisão vem ao encontro das preocupações manifestadas por entidades médicas como a Sociedade Brasileira de Endocrinologia e Metabologia, a Sociedade Brasileira de Diabetes e a Associação Brasileira para o Estudo da Obesidade e da Síndrome Metabólica. As instituições alertam sobre o uso crescente e descontrolado desses medicamentos, muitas vezes sem orientação médica adequada.
“As lacunas na legislação anterior facilitaram o acesso indiscriminado e a automedicação, expondo usuários a riscos desnecessários”, afirmam em nota conjunta.
Prescrição off label permanece válida
A Anvisa esclareceu que a nova regra não interfere no direito médico de prescrever esses medicamentos para finalidades que não constam na bula, prática conhecida como uso off label. A agência reforça que a decisão deve ser feita com consentimento e esclarecimento ao paciente, dentro da responsabilidade clínica.
Alerta contra versões manipuladas
Em fevereiro, as entidades médicas também emitiram alerta sobre o uso de versões alternativas ou manipuladas de semaglutida e tirzepatida – princípios ativos presentes nesses medicamentos. Segundo o comunicado, essas formulações podem apresentar sérios riscos à saúde, por não passarem pelos rigorosos testes de bioequivalência, esterilidade e estabilidade térmica exigidos para produtos injetáveis biológicos.
Entre as recomendações destacadas na nota estão:
Profissionais de saúde devem prescrever apenas medicamentos industrializados e aprovados pela Anvisa;
Pacientes devem rejeitar versões manipuladas ou vendidas em plataformas não regulamentadas;
Anvisa e conselhos médicos devem intensificar ações de fiscalização contra práticas ilegais de comercialização.
A nova medida representa um esforço das autoridades sanitárias para proteger a saúde pública, garantir o uso seguro e responsável desses medicamentos e preservar o acesso dos pacientes que realmente necessitam do tratamento.